

國中組 第二名
縣 市:苗栗縣
校 名:造橋國中
作 者:鄧惠如、盧鴻鈞
劉祐銜、江淑君
指導教師:林明文、邱垂翰

盧鴻鈞:出生於苗栗縣造橋鄉,長的高高的,有時候呆呆的,發表能力特強,有一點點臭屁,他擅長的科目是數學、理化、地理、歷史等,做起事來像瘋子,興趣是看書、打球、打電腦等,他電腦很強,他可日夜顛倒的坐在電腦前打,他每天看起來都像睡眠不足的小鬼!
劉祐銜:出生於苗栗縣造橋鄉,,他很活潑,天天傻笑,又很愛發呆,臉白白的 喜歡講笑話,他性情溫和,但是生氣起來像個野獸,他擅長的科目是國文、理化等,興趣是打電腦、打球、看書等,他永遠看起來都很活潑!
鄧惠如:出生於苗栗縣造橋鄉,因為她長的圓圓胖胖的,很活潑,喜歡搞笑,但是罵起人來很可怕的!她擅長的科目是是數學、理化、歷史等,興趣是打球、睡覺、看書等,她看起來永遠都很有精神!
江淑君:出生於苗栗縣造橋鄉,她很可愛,也很活潑功課也很好!但是罵起人來也挺恐怖的,她擅長的科目是國文、英文、數學、理化等,尤其是他的數學,那可恐怖了,所以她的興趣是算數學、看書、聽音樂等,他永遠看起來都很認真!
關鍵詞:偏光、衰減、酵素
一、研究動機
某日路過實驗室,正巧邱老師在上『葡萄糖加本氏液的呈色實驗』時問道『葡萄糖濃度不同會不會影響加熱後顏色的深淺?』心想著去年,我們測後龍溪河水的濁度的儀器,不正好可以運用。
於是今年我們思考著︰還有哪些光的特性能測得溶液的濃度﹖並希望能用自己動手做出的儀器測得葡萄糖溶液的濃度,深入探討生物課程中『酵素活性』問題。
二、研究目的
(一)討論光的下列物理特性,使用於分辨液體種類與測量液體濃度的適合性︰
(1)光的折射
(2)光的衰減
(3)光的偏振現象
(二)深入探討生物課程中『葡萄糖與本氏液呈色反應』與『酵素活性』問題︰
(1)葡萄糖溶液濃度高低與本氏液反應後呈色的比較
(2)溫度對唾液中酵素活性的影響
(3)酸鹼度對唾液中酵素活性的影響
三、研究設備
我們主要是運用市面上簡便的水電材料,做成我們所需的儀器,分類如下:
器 材
偏光鏡、單色濾鏡、PVC水管、透明壓克力板、照度計、50W鹵素燈泡、12V電瓶、鱷魚夾、溫度計、燒杯、電子秤、量筒、酒精燈、石綿心網、酒精燈架。
試 劑
澱粉、鹽酸(HCl)、氫氧化鈉(NaOH)、唾液、葡萄糖、方糖、本氏液
裝置方式
請參考圖1-4到圖1-6。
四、設計運用原理說明
折 射
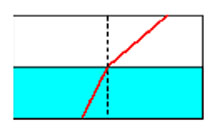
圖1-1 折射原理說明
光線由進入不同介質時,行進方向會被曲折。
光的吸收衰減
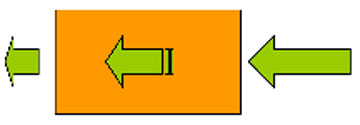
圖1-2 光的吸收衰減
光射入有色液體時會被吸收,使得射出的光強度變弱。
旋 光
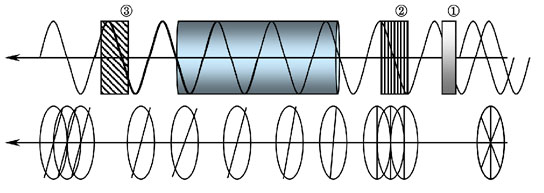
圖1-3 受測分子將光線旋轉說明
偏振光(polarization)進入有旋光性的溶液,振動角度會被改變。
說 明
1.過濾取得單色光線。
2.過濾取得單一振動方向的光線。
3.轉動3號偏光鏡,讀取照度最大值,即代表相同振動方向的光線通過。
4.偏光角度~f(光源強度,光源顏色,路徑長短,受測物種類,受測物濃度)
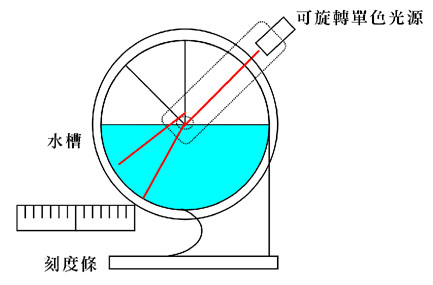
圖1-4 折射率測量裝置
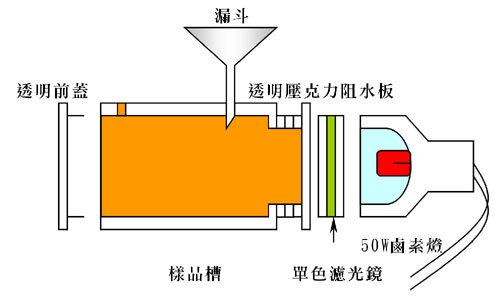
圖1-5 光衰減度測量裝置
註:
1. 使用光源有鎢絲燈光、紅光、藍光、綠光。
2. 刻度條是以,尺影印縮小,貼在水槽下半圓,再計算出每隔代表的角度使用。180/156=1.15 (度/格)
3. 短水槽長度為12.5cm。
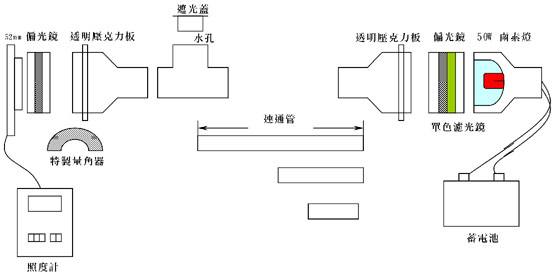
圖1-6 旋光與光衰減共用量測儀設計圖
五、第一部分 溶液的折射
目 的
觀察不同濃度的溶液折射情形是否不同
實驗方法
1.配製20g/100ml、15g/100ml、10g/100ml、5g/100ml的葡萄糖與方糖溶液,倒入折射測量裝置中。
2.以鎢絲燈、紅光、綠光、藍光照射,旋轉光源10至80度的每隔10度紀錄折射角度觀察有何差異。
結 果
1.不同顏色的光之間,折射角度上差異均在1度以內,沒有統計上的意義。(參考葡萄糖數值表,見下表2-1)
2.表2-2中觀察到,數值上並無法有效分辨出同濃度的葡萄糖、蔗糖與果糖溶液。
3.不同濃度的溶液(表2-3),是唯一觀察到有差異的部分,我們可以看到,蔗糖濃度加大4倍後,折射角僅增加2.5度左右。而葡萄糖加大約3度。
表2-1 2g/100ml葡萄糖折射角的比較
入射角 |
折射角度 |
|||
鎢絲燈光 |
紅光 |
藍光 |
綠光 |
|
10 |
5.5 |
5.8 |
4.8 |
5.0 |
20 |
12.9 |
13.7 |
11.9 |
12.8 |
30 |
21.3 |
20.9 |
20.2 |
20.0 |
40 |
25.7 |
26.8 |
26.6 |
25.7 |
50 |
30.7 |
32.4 |
32.5 |
31.0 |
60 |
35.9 |
36.3 |
36.1 |
36.7 |
70 |
42.1 |
40.5 |
40.9 |
40.9 |
80 |
44.8 |
43.9 |
42.8 |
42.9 |
表2-2. 同濃度不同種類溶液折射角的比較
入射角 |
折射角度 |
||
20/100(g/ml)果糖 |
20/100(g/ml)蔗糖 |
20/100(g/ml)葡萄糖 |
|
10 |
5.1 |
6.1 |
5.0 |
20 |
11.9 |
12.2 |
11.5 |
30 |
17.3 |
18.1 |
16.5 |
40 |
23.1 |
23.9 |
22.5 |
50 |
27.5 |
28.1 |
27.2 |
60 |
31.1 |
32.1 |
31.5 |
70 |
33.9 |
35.9 |
34.5 |
80 |
35.1 |
36.6 |
36.5 |
表2-3 高低濃度蔗糖與葡萄糖折射角的比較
入射角 |
折射角度 |
|||
5/100(g/ml) 蔗糖 |
20/100(g/ml) 蔗糖 |
5/100(g/ml) 葡萄糖 |
20/100(g/ml) 葡萄糖 |
|
10 |
4.7 |
7.0 |
4.3 |
5.8 |
20 |
12.8 |
14.1 |
11.1 |
13.3 |
30 |
19.0 |
20.9 |
17.3 |
19.0 |
40 |
25.3 |
27.6 |
22.3 |
26.0 |
50 |
30.6 |
32.4 |
26.9 |
31.4 |
60 |
35.9 |
37.0 |
31.8 |
36.3 |
70 |
38.2 |
41.4 |
35.5 |
39.8 |
80 |
40.3 |
42.2 |
37.2 |
42.1 |
討 論
雖然結果沒有大差異,至少我們知道了,溶液濃度越高折射角越大,但要使用此法時,若濃度未達一定的差距,並無法分辨出濃度的差異,敏感度顯然不足。
未來希望可由下列兩個方法改善結果:
1.提昇角度量測的精密度,如利用顯微鏡觀察折射角。
2.更改入射光所在的介質,應該可以增加折射角度,更有利於觀察。
六、第二部分 葡萄糖溶液的衰減
目 的
1.比較不同濃度溶液的吸光度差異。
2.驗證我們『葡萄糖濃度越高與本氏液加熱後顏色越深』的假設。
實驗方法
1.調製濃度為5g/100ml、10g/500ml、15g/500ml、20g/100ml葡萄糖與方糖溶液。
2.測背景光(P0),再將溶液倒入兩用測定儀器中、長、超長管中,測出光的照度值(P)。
3.算出穿透率及吸光度。
4.將溶液進行與本氏液的呈色實驗後(請參考第四部分實驗1),將液體倒入光徑為12.5cm的小型儀器中,測出光的照度值。
(1)未呈色部分
結 果
由圖3-1中數據觀察到
a.葡萄糖與方糖濃度越高,光線穿透率越低。
b.管徑越長,光線穿透率越低。
比較圖3-1-1與圖3-1-2發現方糖的斜率,比葡萄糖低,顯示方糖未呈色直接測時敏感度較低。

圖3-1 未呈色的葡萄糖與蔗糖溶液於兩用裝置中的光線穿透率
討 論
1.高濃度的量測其實不難,若濃度太高可用下列方法解決:
a.稀釋測量:再依稀釋比例回算。
b.使用短管:使光徑變短,透光率自然增加。
c.加強光源:與使用短管有異曲同工之妙。
d.其他方法取代:偏光法(限有旋光性物質)。
問題在於濃度太低,就必須以 1.使溶液呈色 2.加長管的方法來解決,且感應 裝置必須相當敏感,屬於較困難部分。
2.根據實驗時的觀察,葡萄糖本身會呈微黃色,所以適合未呈色時測量,這也應該是斜率較方糖高的原因。
(2)呈色部分
結 果
1.由數據觀察到結果,濃度越高光的穿透力會越弱。
2.較低濃度的葡萄糖,未呈色時並無法用光減法有效的測量,但顯色後可使偵測極限達到小於0.31g/100ml或更小的地步(圖3-2)。
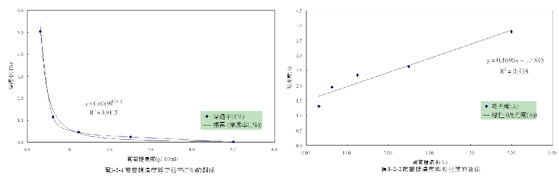
討 論
1.葡萄糖濃度與透光率的關係呈L型的反比曲線,以我們的短管量測器而言,觀察圖中較高濃度時(>1g/100ml)曲線較平坦,此時濃度改變很多透光率才會改變些許屬敏感度較差的區域,低濃度區(<1g/100ml)因斜率較大敏感度較高。為了方便觀察將穿透率(T%)可轉化為吸光度(A),也就是濃度越高光的吸收度會越強,轉換方式如下:

觀察圖3-2-2(右),若將T%轉換成A可得到一線性較好觀察的正比直線,可將葡萄糖濃度每一吸光度互相轉換方程式:
(吸光度A)=04696 ×(葡萄糖濃度)+1.4895 回歸係數(R2)=0.938
2.葡萄糖呈色若反應完全均屬於橙色系,如果用遠離橙色系(互補色)的單色濾鏡將成橙色光濾除,將大大的提高敏感度。
七、第三部分 葡萄糖溶液的偏光角度
目 的
測得不同濃度的溶液的偏光旋轉角度。
實驗方法
1.同第二部分。
2.加溶液前,先歸零,旋轉偏光鏡調到光線最亮時,標示為0。
3.再將溶液倒入兩用測定儀器中、長、超長管中。
4.旋轉偏光鏡至最大照度,讀取旋轉角度值。
結 果
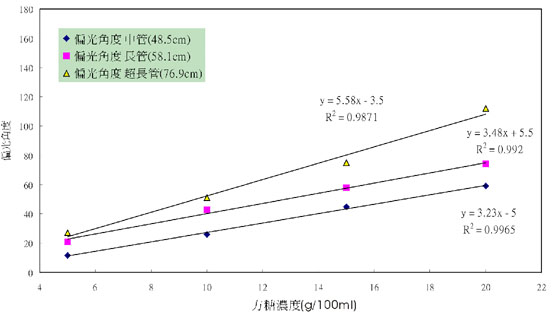
1.濃度越高偏光角度越大。
2.光徑越長偏光角度越大。
3.比較圖3-1與圖4-1,葡萄糖未呈色時用光衰減法的回歸係數範圍0.81~0.97,用旋光分析的回歸係數平均0.99以上,方糖的差異更明顯,所以高濃度時利用旋光性的方法比使用光衰減法好。
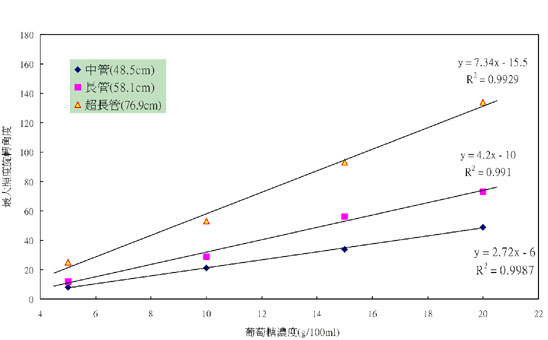
圖4-1 葡萄濃度與旋光角度的關係
討 論
我們曾經測量市售的果糖,結果不是好可能原因應該是:
1.當中含有其他糖類或有旋光性的混合物。
2.旋光角度超過3600。
八、第四部分 生物課程中葡萄糖溶液與本氏液呈色反應的深入探討
實驗1 葡萄糖溶液濃度高低與本氏液反應後呈色的比較
目 的
1.比較不同濃度的葡萄糖溶液反應後顏色的深淺。
2.運用『比色法』測定葡萄糖溶液濃度的高低。
實驗步驟
1.配置5g/100ml,2.5g/100ml,1.25g/100ml,0.63g/100ml,0.31g/100ml的葡萄糖水溶液。
2.將溶液移至酒精燈上加熱至80 以後,加入本氏液5ml,等待5分鐘使其呈色完成。
3.降溫至30 後將溶液倒入測定器內,讀取照度值。
結果與討論
合併於於第二部分
實驗2 溫度對唾液中酵素活性之影響
目 的
唾液中酵素會將澱粉轉化為葡萄糖,將唾液與澱粉混合後在不同溫度反應後,測量葡萄糖的濃度,比較酵素在不同溫度下的活性大小。
實驗步驟
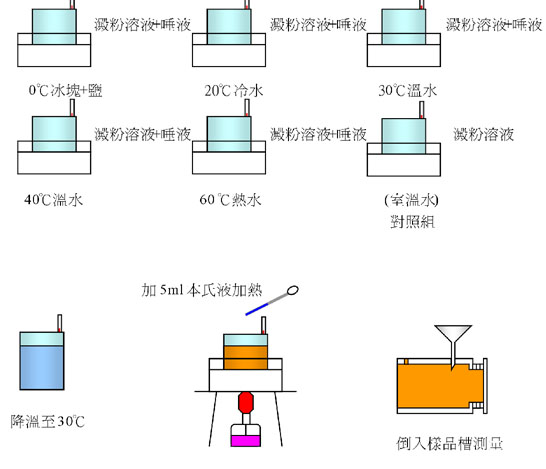
1.將5g的澱粉,倒入6組(一組對照組)標示好的燒杯中加水至500ml攪拌均勻。
2.將燒杯移至調好溫度為0 ,20 ,30 ,40 ,60 的水盆中,待燒杯中溫度計到達指定溫度後,加入8ml的唾液混合(對照組不加唾液)。
3.控制溫度輕微攪拌30分鐘。
4.移至酒精燈上快速加熱至80 加入5ml的本氏液,使其呈色。
5.降溫至30 後將溶液倒入測定器內,讀取照度值。
結 果
1.反應後若溶液中葡萄糖濃度越高代表酵素活性大,實驗結果顯示,40 時酵素活性最大,往低溫及高溫環境活性均會降低。
2.0 時因加入溶液後光強度大於對照組所以不列入分析。
3.濃度推算方式,是利用第二部分中的葡萄糖呈色濃度與光的吸收度的回歸方程式求得。
表5-1 不同溫度下唾液中酵素將澱粉轉換葡萄糖濃度
光源 |
溶液 種類 |
溫度 (0C) |
距離 (cm) |
背景光 (1ux) |
加入樣品後 光強度(1ux) |
透光率(T%) |
吸光度(A) |
推算濃度(xg/100ml) |
50W |
唾液+澱粉+本氏液 |
20 |
12.5 |
129900 |
1820 |
1.40 |
1.85 |
0.78 |
30 |
12.5 |
162600 |
206 |
0.13 |
2.90 |
3.00 |
||
40 |
12.5 |
162400 |
93 |
0.06 |
3.24 |
3.73 |
||
60 |
12.5 |
166300 |
332 |
0.20 |
2.70 |
2.58 |
討 論
在此我們可以非常清楚的知道,酵素在略高於人體溫度37 附近活性最大,太高或太低的溫度均不適合酵素進行分解,難怪在較熱的天氣下食物容易腐臭。
目 的
比較酵素在不同酸鹼度下的活性大小。
實驗步驟
1.將2M的NaOH與2M的HCl稀釋10-5,10-2,10-1倍,各500ml。
2.將5g的澱粉在加入六組燒杯中,加以上溶液至500ml攪拌均勻,對照組與其中一組保持中性。
3.將燒杯移至40 的水盆中,加入8ml的唾液混合(對照組不加唾液)。
4.控制溫度輕微攪拌30分鐘。
5.移至酒精燈上快速加熱至80 加入5ml的本氏液,使其呈色。
6.降溫至30 後將溶液倒入測定器內,讀取照度值。
結 果
1.中性環境下葡萄糖的產量高達2.81g/100ml。弱酸(PH=5)與弱鹼(PH=9)環境下,呈色反應程度下降,代表了唾液中的酵素活性降低。
2.當PH小於2(強酸性)時,與PH大於12(鹼性)沒有葡萄糖反應,代表酵素沒有活動跡象。
表5-2 不同酸鹼度下唾液中酵素將澱粉轉換葡萄糖濃度
光源 |
溶液 種類 |
環境 特性 |
距離 cm |
背景光 1ux |
加入樣品後 光強度(1ux) |
透光率(T%) |
吸光度(A) |
推算濃度xg/100ml |
50W |
唾液+澱粉+本氏液 |
PH<2 |
12.5 |
153400 |
92900 |
60.56 |
0.22 |
0.00 |
PH=2 |
12.5 |
168400 |
2053 |
1.22 |
1.91 |
0.90 |
||
PH=5 |
12.5 |
163800 |
803 |
0.49 |
2.31 |
1.75 |
||
PH=7 |
12.5 |
167800 |
260 |
0.15 |
2.81 |
2.81 |
||
PH=9 |
12.5 |
152400 |
603 |
0.40 |
2.40 |
1.94 |
||
PH=12 |
12.5 |
165800 |
1853 |
1.12 |
1.95 |
0.98 |
||
PH>13 |
12.5 |
168200 |
15470 |
9.20 |
1.04 |
0.00 |
註:對照組光強度為1878Lux
討 論
用鹽酸代表所有的酸性物質或許武斷,因此有機會我們想比較其他酸性物質(如硝酸,硫酸等)所組成的酸性環境對酵素活性的影響,在此先證明了酵素活性會受酸鹼性的影響。
未來希望以精密的PH計,再次確定微弱酸與微鹼環境酵素的活動力。另外若能將方法的敏感度增強,我們想用於觀察植物受酸雨影響的光合作用情況。
九、結論
1.不同種類的糖溶液無法用折射率來分辨,且不同濃度的溶液,折射角變化也不大。所以溶液折射角最多只適合辨認濃度相差極大的溶液,基於改變程度極低,不建議發展此類儀器。
2.利用光的衰減測濃度,適合應用於有色溶液與高濃度的葡萄糖,如果要測無色或低濃度糖溶液,需將溶液呈色。有色溶液中呈色較深者測定濃度適用短管,呈色較淺者適用長管。
3.葡萄糖濃度越高,呈色顏色越深。
4.利用葡萄糖的旋光性,所發展的儀器,濃度與偏光角度的線性關係非常良好。
4-1濃度高者,偏光角度越大,適合用短的管子測定。
4-2濃度低者,偏光角度越小,適合用長的管子測定。
5.唾液中的酵素活性最高時溫度為40 ,低溫時酵素呈休眠狀態,高溫時接近70 為蛋白質凝固點,酵素活性降低。
6.PH值為7(中性)時酵素活性最大,隨酸鹼性增加唾液中酵素活性會逐漸降低,在強酸與強鹼環境下酵素作用停止。
7.在衰減的實驗中,用與溶液互補色的光線做實驗,可提高實驗準確性與敏感度,旋光實驗中使用單色光,亦可提高實驗準確性與敏感度。
十、參考文獻
1.國中理化第一冊 國譯編譯館
2.國中生物第一冊 國譯編譯館
3.分析化學 闕山仲 藝軒出版
4.儀器分析
評語
本作品利用光的折射、衰減與偏振來測定葡萄糖的濃度,並據以研究酵素之活性。測量用的工具係作者自行構思製作,且量測的方式與數據,充份反應作者對工具的掌握與應用。惜美中不足之處在作者並未了解主要是葡萄糖的光活性(optical actirity),而非雙折射性(bi-refringence)造成光偏極化狀態的改變。但對光偏振的詳細描述與理論確已遠超出國中生了解之範籌。
附註:
(1)雙折射係指對不同偏振方向的光折射率的不同。
(2)光活性(optical actirity)特指對左旋光與右旋光折射率的不同。
回到目錄頁../Index.htm